BRAF V600E突变型转移性结直肠癌具有独特的生物学行为和临床表现,其侵袭性强、生存期短,传统化疗疗效有限。单一的BRAF抑制剂疗法在结直肠癌中疗效欠佳,一方面因肿瘤细胞存在EGFR信号反馈激活机制,导致BRAF信号通路快速重新激活,降低单药抑制效果。前期BEACON CRC研究确立了Encorafenib与Cetuximab联合用于既往治疗失败后的BRAF V600E突变结直肠癌标准二线及以上治疗方案,但一线治疗领域尚无明确优选方案。
6月26日,发表在国际顶刊《新英格兰医学杂志》的一项BREAKWATER III期临床试验,探讨了将BRAF抑制剂Encorafenib与抗EGFR单抗Cetuximab联合mFOLFOX6化疗的一线治疗效果,首次全方位公布了无进展生存及总生存的中期及更新数据。此项国际多中心随机开放标签试验纳入了未经治疗的BRAF V600E突变转移性结直肠癌患者,比较了上述联合方案与标准治疗(包含不同化疗方案,±贝伐单抗)的疗效与安全性,为该亚型患者提供了新的治疗策略依据。

BREAKWATER为一项多国多中心随机对照开放标签3期临床试验,纳入未经全身治疗的BRAF V600E突变转移性结直肠癌患者。患者采用1:1:1随机分配接受Encorafenib+Cetuximab(EC)、EC+mFOLFOX6或医生选择的标准治疗组(多为含贝伐单抗的多种化疗方案)。主要终点包括盲法独立中心评估的客观反应率(已早期报道)及无进展生存期(PFS),次要终点为总生存期(OS)、安全性及患者报告结果。统计学设置保证足够的事件数在单侧0.023的显著性水平下检验PFS差异,同时采用分层Cox模型调整分层因素。
结果显示,
患者基线特征
| 特征 | EC组 (N=158) | EC+mFOLFOX6组 (N=236) | 标准治疗组 (N=243) |
|---|---|---|---|
| 中位年龄(岁) | 59 | 60 | 62 |
| 女性比例 | 50.0% | 47.9% | 51.0% |
| 肿瘤部位(右结肠) | 56.3% | 61.9% | 59.7% |
| 肝转移存在者 | 59.5% | 62.3% | 65.8% |
| ECOG 0评分(状态好) | 50.0% | 54.2% | 53.9% |
| BRAF V600E突变验证(中央) | 94.9% | 95.8% | 92.2% |
无进展生存期(PFS)
- EC+mFOLFOX6组中位PFS为12.8个月,显著优于标准治疗组7.1个月(HR=0.53,95% CI 0.41-0.68,P<0.001)。
- EC单药组中位PFS为6.8个月。
- 各亚组包括不同年龄、性别、肿瘤部位、肝转移与否均显示一致的PFS获益(见Fig1)。
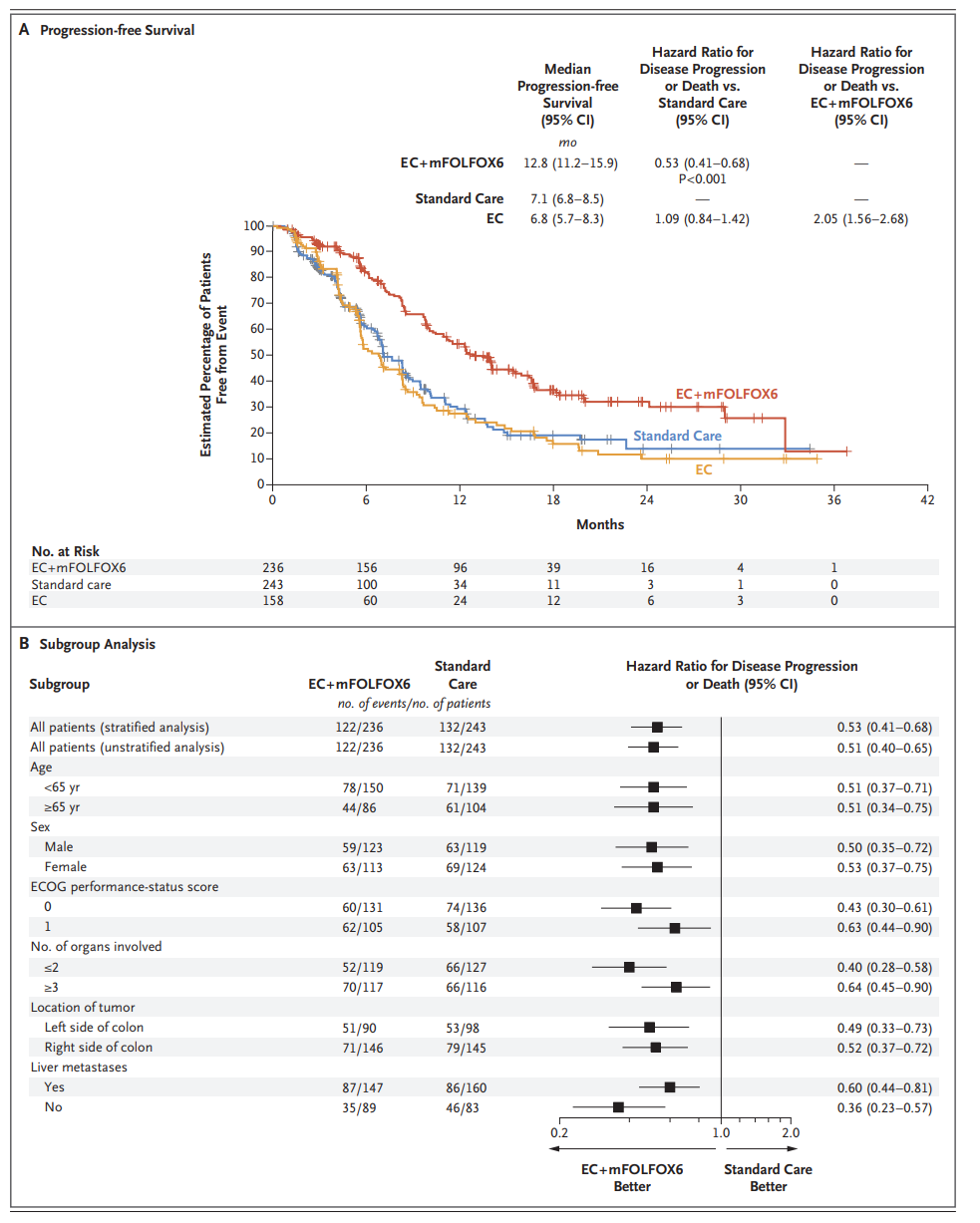
图:无进展生存期(PFS)Kaplan–Meier曲线及亚组分析
总生存期(OS)
- 截至数据截止,EC+mFOLFOX6组中位OS达到30.3个月,远超标准治疗组15.1个月(HR=0.49,95% CI 0.38-0.63,P<0.001)。
- 1年及2年生存率在联合治疗组分别为80.1%和52.0%,显著优于标准治疗组(66.0%和29.0%)。
- EC单药组中位OS为19.5个月。
- 多数亚组均显示总生存优势。
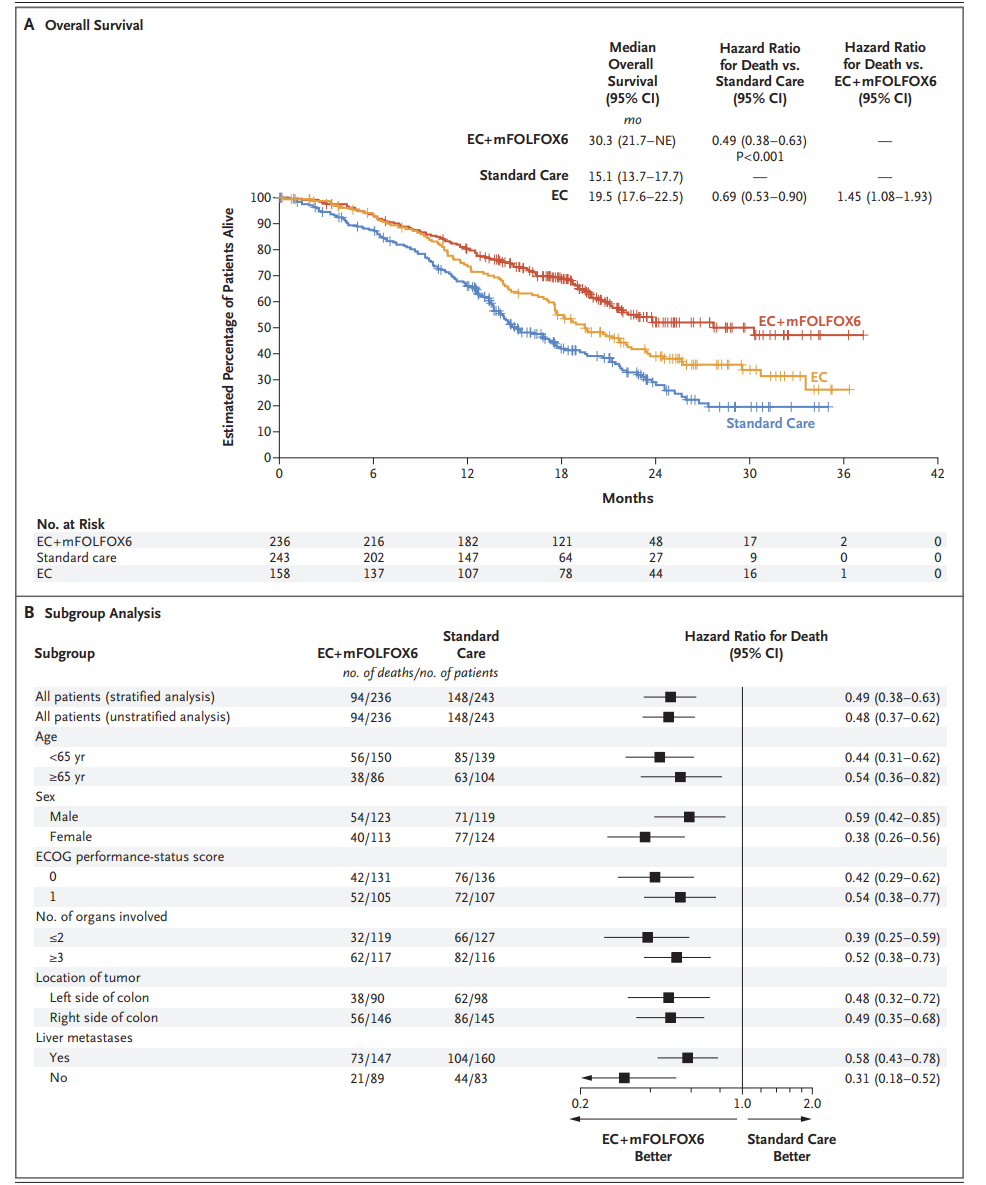
图:总生存期(OS)Kaplan–Meier曲线及亚组分析
客观缓解率(ORR)与缓解特征

安全性分析
- EC+mFOLFOX6组治疗期间三/四级不良事件发生率为81.5%,标准治疗组为66.8%,EC组为42.5%。
- 严重不良事件发生率(≥3级)最高见于联合组46.1%,标准组38.9%,EC组30.1%。
- 死亡相关不良事件发生率相近,各组约2-4%。
- 联合组较高副作用主要与化疗相关,药物特异性毒性符合既往认识,无新安全性信号。
- 不良事件导致永久停药率联合组约26.7%,标准组17.5%,化疗剂量减量也较高但均可接受。
后续治疗及二线无进展生存
- 约六成患者在一线进展后接受后续治疗,标准组中大部分接受BRAF抑制相关方案。
- 二线PFS中位数:联合组20.7个月,标准组12.7个月,EC组14.3个月,显示整体治疗序列获益潜力。
研究价值与未来展望
BREAKWATER试验首次通过3期高水平循证数据证实了以通路激活机制为靶点的多药联合治疗能显著改善BRAF V600E突变转移性结直肠癌患者一线疗效,尤其是在无进展生存和总生存方面。在以往预后极差的群体中,联合方案将死亡风险减少近50%,极大延长了患者生命期,这一发现有望改变临床实践指南。值得注意的是,该方案虽伴有较高的三、四级不良事件,但总体安全性可控,不良事件管理得当。未来可进一步探索替代化疗方案(如FOLFIRI)与双靶向联合策略的比较,或联合免疫治疗以覆盖更多分子亚型,如MSI-H/dMMR BRAF突变患者。同时,对耐药机制的深入剖析及个体化精准医疗的新方法开发,将进一步推动该领域进步。
原始出处
Encorafenib, Cetuximab, and mFOLFOX6 in BRAF-Mutated Colorectal Cancer.New England Journal of Medicine, 2025 Jun 26; 392(24): 2425-2437. DOI: 10.1056/NEJMoa2501912.




