新辅助治疗是Ⅱ、Ⅲ期人表皮生长因子受体2(HER2)阳性乳腺癌的标准治疗方案,其中紫杉醇类药物联合曲妥珠单抗、帕妥珠单抗加卡铂(TCbHP)的方案在临床广泛应用。但卡铂带来的血液学毒性的等不良反应,常导致治疗剂量调整或中断,影响患者治疗依从性与生活质量。
2026年一项发表于《Journal of Clinical Oncology》的Ⅲ期非劣效性试验(neoCARHP),通过对比紫杉醇类药物联合双靶(曲妥珠单抗+帕妥珠单抗,THP)与TCbHP方案的疗效与安全性,为HER2阳性乳腺癌新辅助治疗的去铂化策略提供了高质量证据。
研究核心
neoCARHP研究是一项多中心、随机、开放标签的Ⅲ期非劣效性研究,纳入2021年4月至2024年8月期间774例未经治疗的Ⅱ、Ⅲ期HER2阳性浸润性乳腺癌患者,按1:1随机分为THP组(387例)与TCbHP组(387例),最终766例患者纳入改良意向治疗(mITT)人群(THP组382例,TCbHP组384例)。两组均接受6个3周周期治疗,THP组采用研究者选择的紫杉醇类药物(多西他赛、紫杉醇或白蛋白结合型紫杉醇)联合曲妥珠单抗+帕妥珠单抗,TCbHP组在此基础上加用卡铂。
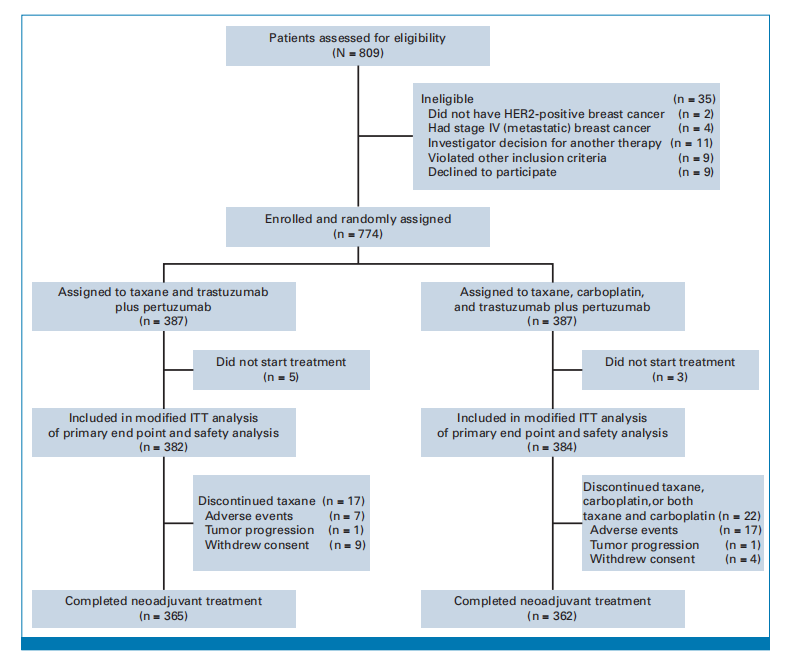
图1.neoCARHP研究的人群
研究主要终点为乳腺及腋窝病理完全缓解率(pCR,ypT0/is ypN0),非劣效性边际设定为-10%。结果显示,THP组pCR率为64.1%(95%CI:59.1%-69.0%),TCbHP组为65.9%(95%CI:60.9%-70.6%),两组绝对差异为-1.8%(95%CI:-8.5%-5.0%),非劣效性检验P值为0.0089,证实THP方案疗效不劣于TCbHP方案。
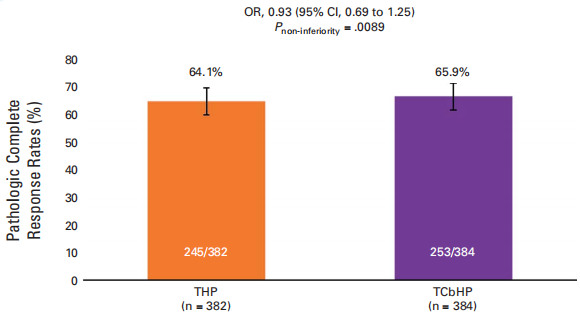
图2.改良意向治疗(mITT)人群中的pCR
安全性方面,THP组3-4级不良事件发生率(20.7%)显著低于TCbHP组(34.6%),严重不良事件发生率(1.3%)也低于TCbHP组(4.7%),其中中性粒细胞减少、白细胞减少等血液学毒性的差异最为明显,且两组均无治疗相关死亡。亚组分析显示,无论激素受体(HR)状态、淋巴结状态、肿瘤分期如何,THP方案均保持非劣效性。
这一系列研究数据,不仅直接回答了“去铂化是否可行”的核心问题,我们更可从乳腺癌诊疗实践、药物治疗研发与应用、临床研究与精准医疗等多个维度,挖掘该研究带来的深层启发与实践价值。
疗效与生活质量的平衡理念深化
乳腺癌治疗已从“追求疗效”向“疗效与生活质量并重”转变,neoCARHP研究的结果契合这一趋势。THP方案显著降低了3-4级血液学毒性、胃肠道反应等发生率,减少了粒细胞集落刺激因子(G-CSF)的使用需求,不仅降低了治疗相关并发症风险,还减轻了患者的身体痛苦与经济负担,有助于提升患者治疗依从性和术后生活质量,为乳腺癌综合治疗的人文关怀提供了实践支撑。
药物治疗中毒性管理的优化方向
TCbHP方案的主要毒性集中在血液学系统,而THP方案通过去除卡铂,显著降低了中性粒细胞减少、血小板减少等风险,提示在药物治疗中,应重点关注“高毒性药物的必要性评估”。
neoCARHP研究的其他参考价值
-
临床研究设计:neoCARHP研究采用非劣效性设计,精准聚焦“去铂化策略的疗效与安全性”,在靶向治疗时代,针对“药物精简”“方案优化”的研究,可借鉴该研究的非劣效性设计思路,明确新方案的疗效边界,为临床实践提供可靠证据。
-
卫生经济学:卡铂作为临床常用化疗药物,虽价格相对低廉,但长期使用需配合G-CSF等支持治疗,且不良反应导致的治疗中断、并发症处理等,均增加了医疗成本。THP方案去除卡铂后,不仅减少了药物本身的费用,还降低了支持治疗及并发症处理的成本,从卫生经济学角度而言,可减轻医疗系统与患者的经济负担,尤其适合在资源有限的地区推广,提升乳腺癌治疗的可及性。
-
科研思路:该试验为后续研究指明了方向:一方面,可进一步探索去铂化方案在更广泛人群中的适用性(如转移性HER2阳性乳腺癌、老年患者、合并基础疾病患者);另一方面,可结合新型治疗手段(如抗体药物偶联物ADC),探索“去化疗”或“进一步减毒”的可能,为患者提供更精准、低毒的治疗选择。此外,该试验的多中心研究模式,也为我国肿瘤临床研究的规范化开展提供了参考,有助于提升我国肿瘤研究的国际影响力。
总结与展望
在肿瘤治疗日益精准的今天,"做减法"往往比"做加法"更需要勇气和智慧。neoCARHP研究为部分HER2阳性乳腺癌患者提供了更安全、更易耐受的治疗选择,同时证明,通过严谨的科学设计和高质量的临床证据,我们可以在保证疗效的前提下,为患者减少毒性负担,深刻体现了肿瘤治疗领域“以人为本、精准医疗”的人文关怀与智慧。
参考文献
1.Wang K, et al. Neoadjuvant Taxane Plus Trastuzumab and Pertuzumab With or Without Carboplatin in HER2-Positive Breast Cancer: The neoCARHP Randomized Clinical Trial. J Clin Oncol. 2026 Jan 23.
2.von Minckwitz G, et al. Trastuzumab Emtansine for Residual Invasive HER2-Positive Breast Cancer. N Engl J Med. 2019.
3.中国抗癌协会乳腺癌专业委员会。中国抗癌协会乳腺癌诊治指南与规范(2025版). 中华肿瘤杂志. 2025.




