针对实体瘤的mRNA疗法的临床开发
发表时间:2023-07-28 00:00:00
信息来源:梅斯医学
访问次数:153
针对实体瘤的mRNA疗法的临床开发
近年来,基于mRNA的治疗方法已成为生物制药行业的热点。该领域的版图正在从传染病扩展到癌症,需要对其进行总结,以便为行业和研究机构提供数据支持。基于Trialtrove数据库,对1999年-2021年的108项临床试验进行了回顾性分析。已经证明,针对实体瘤的mRNA的临床开发仍处于早期阶段。从树突细胞到基于脂质的平台的递送系统以及从固定肿瘤抗原到个性化新抗原的编码策略都有演变。辅助或维持治疗以及与检查点抑制剂的联合治疗正在成为主要的临床发展方向。

自COVID-19疫苗临床应用以来,基于信使RNA(mRNA)的治疗方法成为近年来生物制药行业的热点。具有制备个性化、生产快速、免疫原性好等优点,mRNA的治疗领域正在扩展到癌症。数十项临床试验已启动并取得初步结果。该篇文章对目前的研究进展进行了总结,对未来的临床发展提出了建议,并为行业和研究机构提供了数据支持。基于Trialtrove数据库,截至2021年12月31日,全球共确定了108项针对实体瘤的mRNA疗法的临床试验。
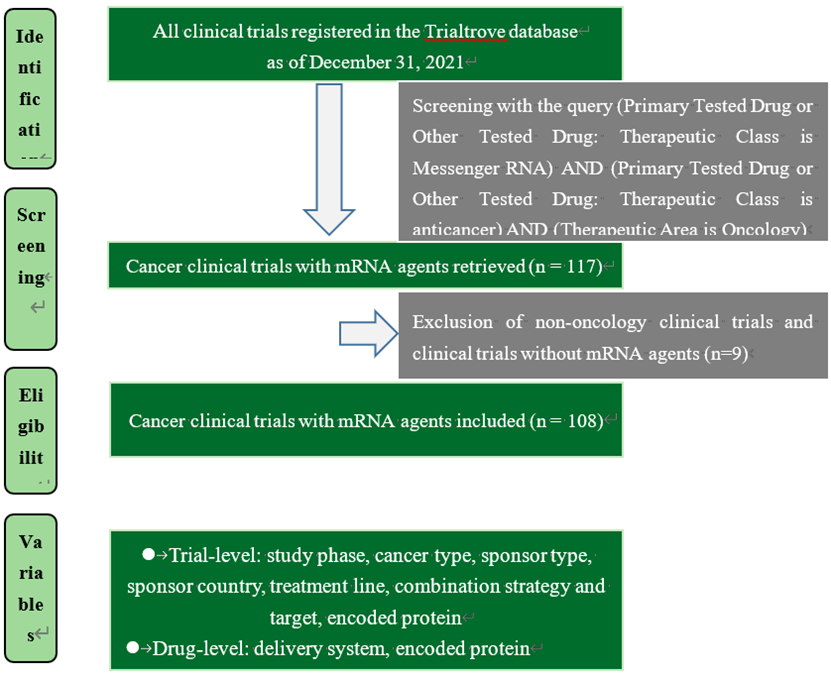
但是目前大多数试验处于第一阶段(79,73.1%),研究者启动的探索性临床试验(IIT)占很大比例(49,45.4%),赞助商高度集中在少数国家,这表明该领域的临床发展仍处于早期阶段。因此,提出了许多挑战和不确定性,包括如何优化信使核糖核酸序列的递送系统和编码蛋白,以及如何选择临床方案。
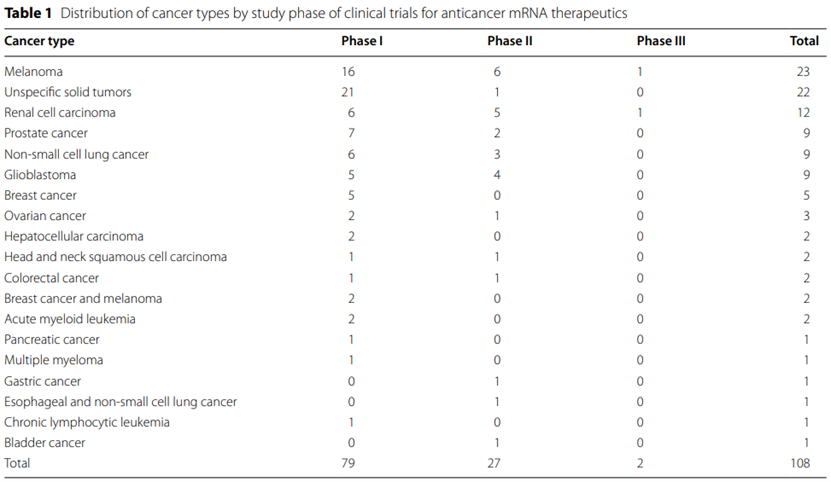
1、mRNA中基于脂质的递送系统技术成为主流
该研究分析了递送系统,脂质基平台,即脂质纳米颗粒(LNP)(13,22.8%)、阳离子脂质复合物(LPX)(8,14.0%)和脂质多聚复合物(LPP)(6,10.5%),合计占比最大(27,47.4%)。树突状细胞(DC)是1999年至2014年开发药物的主要平台(15/25,60.0%),与DC相比,基于脂质的递送系统能够快速生产,具有高可塑性、转染率和免疫原性。因此,该技术自2015年以来已成为主流(27/30,90.0%)。鉴于分子结构的复杂性,进一步优化制造工艺,降低不可预测的临床效果将是脂质基平台的未来发展方向。
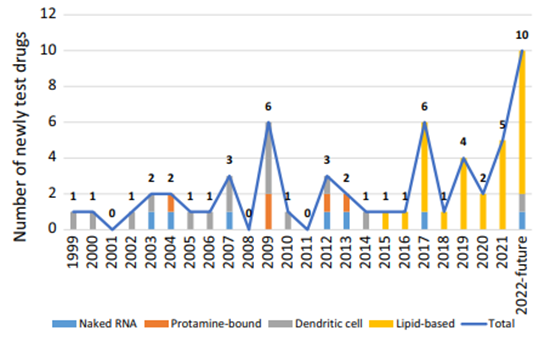
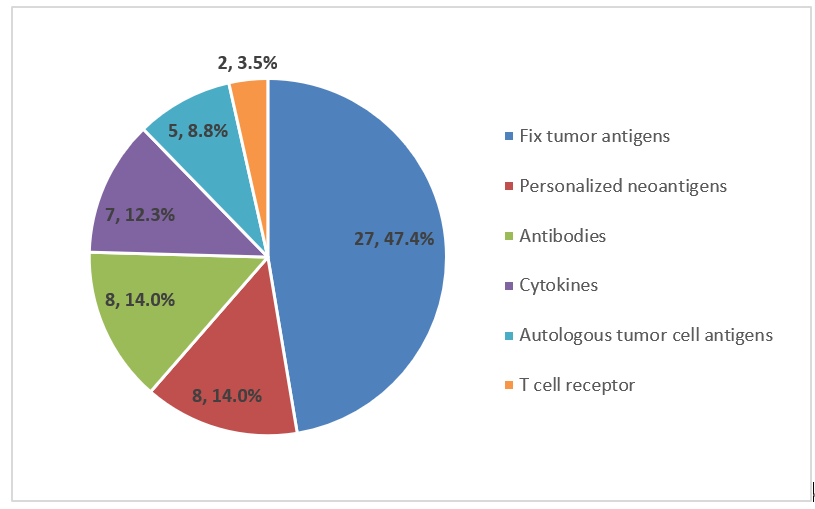
2、mRNA疗法中最常见的编码类别与特异性编码蛋白质
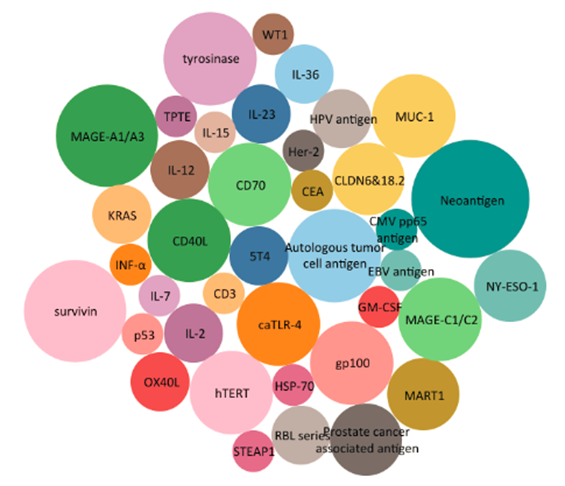
肿瘤抗原是mRNA疗法中最常见的编码类别。分别有27种(47.4%)、8种(14.0%)和5种(8.8%)试剂编码固定肿瘤抗原、新抗原和自体肿瘤细胞抗。MAGE-A1/A3(6,10.5%)、存活蛋白(6,10.5%)和酪氨酸酶(5,8.8%)是最常见的特异性编码蛋白。这与研究最广泛的癌症类型(如黑色素瘤)的特征一致。然而,由于免疫原性不足和经典肿瘤抗原的时空异质,编码固定单一抗原的mRNA药物尚未显示出明确的临床益处。
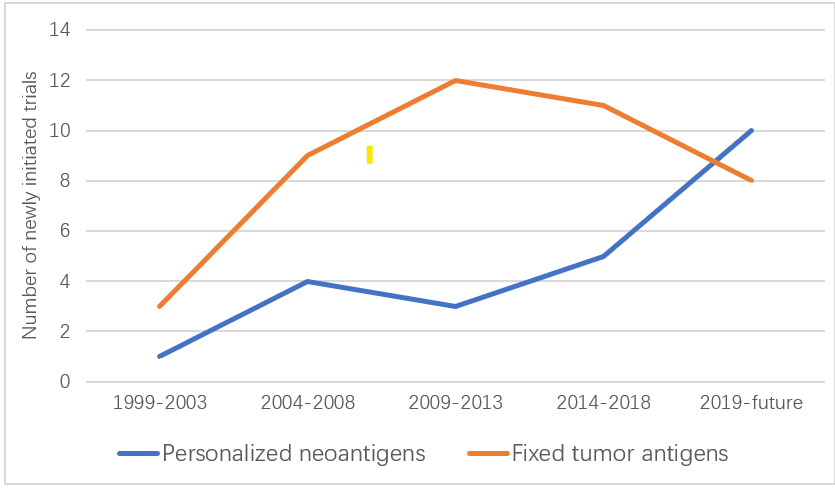
基于新抗原的个性化疗法有望克服这些障碍。随着生物信息学技术的发展,这些高度个性化产品非常适合mRNA的快速生产。自2009年以来,新启动的基于新抗原的药物试验数量已显示出超过固定抗原的趋势(如图5所示)。代表性的mRNA-4157和BNT-122已经取得了有希望的短期疗效,但新抗原预测系统的可靠性和mRNA序列对多种抗原的编码能力仍有待研究。
3、mRNA疗法充当“助手”参与辅助、维持治疗以及联合治疗
在108项试验中,有32项(29.6%)用于辅助或维持治疗,59项(54.6%)涉及联合治疗,其中免疫疗法是最普遍的联合策略(44/59,74.8%)。与免疫肿瘤学的整个景观相比,上述比例相对较高,这推断mRNA药物可能在癌症治疗中充当“助手”而不是“骨干”。此外,参考免疫检查点抑制剂(ICIs)的基本原理,编码肿瘤抗原的mRNA疗法更有可能在癌症早期或晚期发挥更大的作用,肿瘤负荷较低,与ICI产生更大的协同作用。因此,辅助和联合治疗是mRNA治疗临床场景的趋势。
讨论&小结
综上所述,针对实体瘤的mRNA疗法的临床开发仍处于早期阶段。递送系统从DC到基于脂质的平台以及编码策略从固定肿瘤抗原到个性化新抗原的显着转变共同标志着该领域的新时代。辅助或维持治疗与ICIs的联合治疗正在成为重要的临床开发方向。
参考文献:
Wu D, et al. 2023. Clinical development of mRNA therapies against solid tumors. J Hematol Oncol 16:75.


